Vacinação de crianças: governo não tem prazo para iniciar aplicações
"Ainda é preciso ser feita uma análise", disse o ministro da Saúde
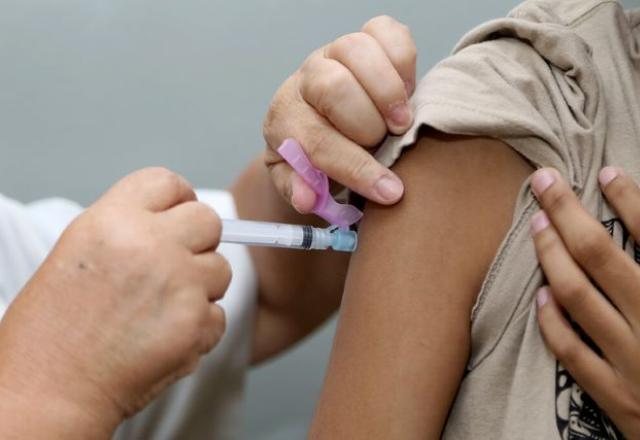
Mesmo com a aprovação da Agência Nacional de Vigilância Sanitária (Anvisa), o Ministério da Saúde ainda não estabeleceu prazos para o início das aplicações da vacina da Pfizer em crianças de 5 a 11 anos de idade.
+ Leia as últimas notícias no portal SBT News
Em conversa com jornalistas na 5ª feira (17.dez), o ministro da Saúde Marcelo Queiroga disse que "ainda é preciso ser feita uma análise" para que se inicie a vacinação. "A avaliação da Anvisa é uma avaliação, a avaliação feita pela câmara técnica do ministério é outra. O ministério vai discutir amplamente esse assunto com a sociedade", afirmou.
À CNN, Queiroga afirmou que fará uma audiência pública para discutir se o Brasil adotará ou não a vacinação contra covid-19 para crianças entre 5 e 11 anos. Audiências públicas são reuniões realizadas com a participação de cidadãos, órgãos e entidades públicas ou civis para tratar temas de interesse público.
O anúncio de autorização da Anvisa, feito de forma online, contou com a presença de diretores e gerentes da agência, que trouxeram pesquisas e análises feitas pelo órgão para a decisão da autorização do imunizante para a população pediátrica. Também participaram representantes da sociedade médica. A vacina da Pfizer para crianças não é a mesma já disponível para os adultos. Segundo a Anvisa, a composição e formulação do imunizante são diferentes, por exemplo, a dosagem da vacina.
De acordo com Gustavo Mendes, gerente geral de medicamentos da Anvisa, o perfil de segurança da vacina quando comparado ao placebo é positivo, sem uma diferença importante entre o placebo e o imunizante. Além disso, não há registro de evento adverso grave.
A aprovação da vacina pela Anvisa foi feita após a definição de uma série de compromissos assumidos pela farmacêutica Pfizer, são eles: submissão de dados complementares, realização de treinamento para profissionais de serviços de vacinação, uso de coloração laranja para doses pediátricas e conduções de ações específicas de comunicação de risco para pais e responsáveis, profissionais da saúde e sociedades científicas. Além disso, a notificação de eventos adversos graves devem ser feitos em até 72h para a Anvisa.










